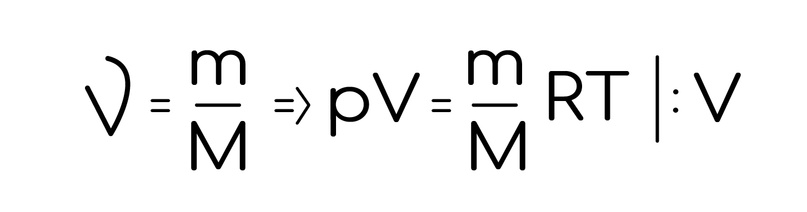У вас большие запросы!
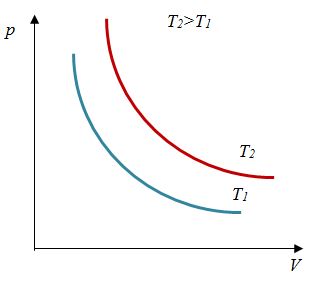
Объединяя законы Бойля - Мариотта и Гей-Люссака уравнения 1 и 2 , можно получить следующее уравнение:. Он позволяет вычислить, например, объем газа при определенных температуре и давлении, если известен его объем при других значениях температуры и давления. Точное значение постоянной в правой части этого уравнения зависит от количества газа.


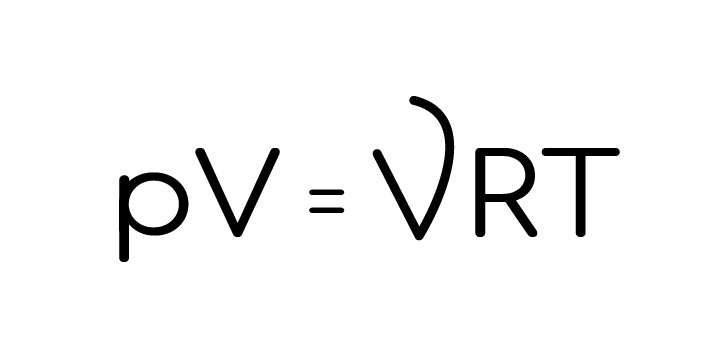









Уравнение состояния идеального газа иногда уравнение Клапейрона или уравнение Клапейрона — Менделеева — формула, устанавливающая зависимость между давлением , молярным объёмом и абсолютной температурой идеального газа. Уравнение имеет вид:. Так как , где — количество вещества , а , где — масса, — молярная масса , уравнение состояния можно записать:. Последнее уравнение называют объединённым газовым законом.



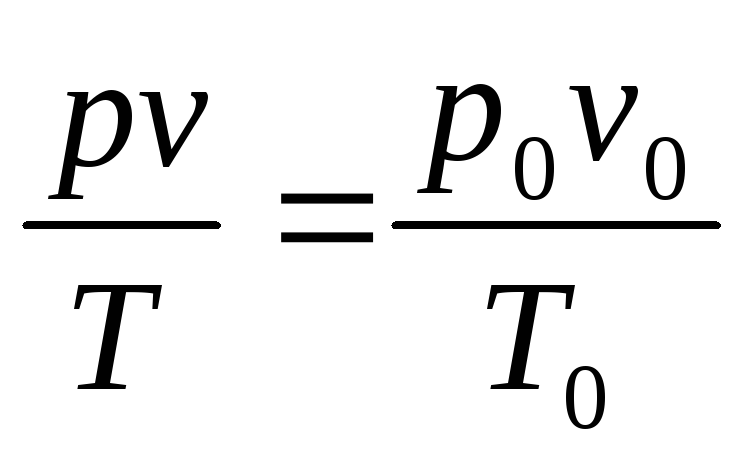




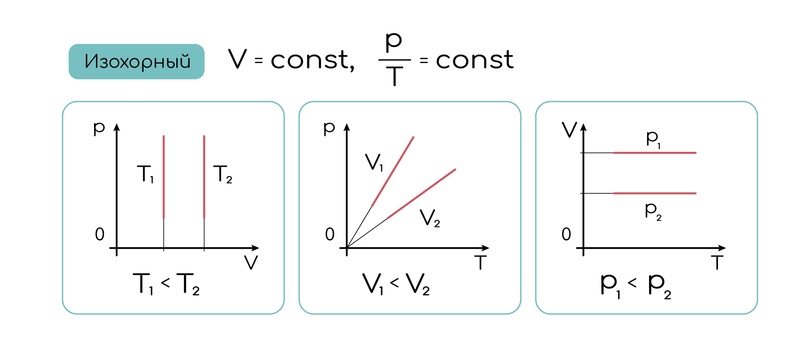
Урок физики в 10 классе по теме:. Тип урока: урок изучения и первичного закрепления новых знаний. Дидактическая цель: ввести понятие «изопроцесс», изучить газовые законы. Образовательные: изучить газовые законы; формировать умение объяснять законы с молекулярной точки зрения; изображать графики процессов; начать обучение учащихся решать графические и аналитические задачи, используя уравнение состояния и газовые законы; установление межпредметных связей физика, математика, биология. Воспитательные: продолжить формирование познавательного интереса учащихся; в целях интернационального воспитания обратить внимание учащихся, что физика развивается благодаря работам ученых различных стран и исторических времен; продолжить формирование стремления к глубокому усвоения теоретических знаний через решение задач.